
Szczepionka przeciw COVID-19
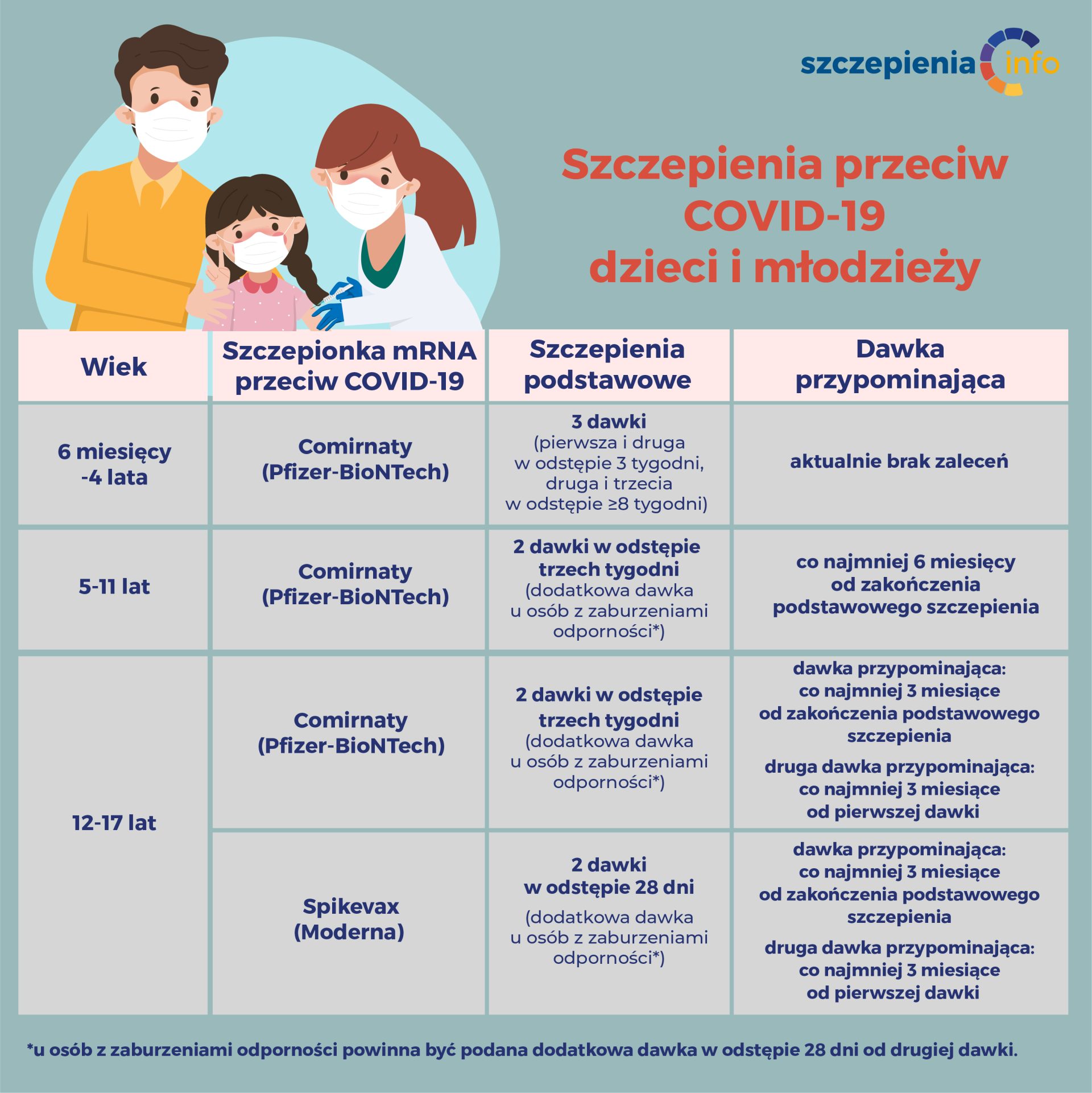
Jaką szczepionkę przeciw COVID-19 podajemy dla dzieci i młodzieży?
Schemat szczepienia przeciw COVID-19 osób z zaburzeniami odporności
Osoby z chorobami towarzyszących, np. onkologicznymi lub z powodu przyjmowanych leków immunosupresyjnych mogą słabiej odpowiadać na szczepienie.
Osoby z zaburzeniami odporności powinny zostać zaszczepione 3 dawkami szczepionki w schemacie podstawowym oraz dwoma dawkami przypominającymi (łącznie 5 dawek szczepionki).
Osoby z ciężkimi zaburzeniami odporności:
- wynikającymi z leczenia przeciwnowotworowego,
- po przeszczepie,
- z umiarkowanym lub ciężkim zespołem pierwotnych niedoborów odporności,
- zakażone wirusem HIV,
- leczone dużymi dawkami kortykosteroidów lub lekami hamującymi odpowiedź immunologiczną,
- dializowane przewlekle z powodu niewydolności nerek,
należą do grupy ryzyka ciężkiego przebiegu COVID-19. Ze względu na chorobę podstawową mogą słabiej odpowiadać na szczepienie przeciw COVID-19 i odpowiedź odpornościowa na podstawowe szczepienie (2 lub 1 dawka w zależności od preparatu) w tej grupie, z wysokim prawdopodobieństwem jest niewystarczająca.
Stąd też zaleca się aby osoby ze wskazanych grup ryzyka były szczepione przeciw COVID-19 w schemacie, który obejmuje podanie łącznie 5 dawek szczepionki:
szczepienie podstawowe:
- 2 dawki podane zgodnie ze wskazaniami dla wieku,
- dawka dodatkowa (inaczej uzupełniająca) podana po co najmniej 28 dniach od drugiej dawki szczepionki.
szczepienie przypominające:
- 1. dawka podana po co najmniej 3 miesiącach od podania dawki dodatkowej,
- 2. dawka podana po co najmniej 3 miesiącach od podania pierwszej dawki przypominającej.
Dodatkową dawkę stosuje się we wskazanych grupach z zachowaniem odstępu co najmniej 28 dni po zakończeniu realizacji schematu szczepienia pierwotnego przeciw COVID-19.
- podajemy szczepionkę Comirnaty (Pfizer-BioNTech) (pełna dawka 30 µg- 0,3 ml)
- lub szczepionkę Spikevax (Moderna) (pełna dawka 100 µg- 0,5 ml), z uwzględnieniem w pierwszej kolejności podania szczepionki determinowanej szczepieniem podstawowym,
Jako dawkę przypominającą u osób z zaburzeniami odporności w wieku ≥ 12 lat można stosować szczepionki:
- Comirnaty (Pfizer-BioNTech) (pełna dawka 30 µg- 0,3 ml)
- Spikevax (Moderna) (połowa dawki 50 µg- 0,25 ml)
Osoby z ciężkimi zaburzeniami odporności szczepione są z wyboru szczepionkami mRNA. Szczepionka COVID-19 Vaccine Janssen może być jedynie warunkowo podana jako heterologiczna dawka przypominająca po szczepieniu podstawowym z dawką dodatkową, wykonanym szczepionką mRNA przeciw COVID-19 u osób powyżej 18 r.ż.
Szczepienia u osób z zaburzeniami odporności są dobrze tolerowane. Rodzaje i częstość występowania działań niepożądanych po szczepieniu jest podobna jak w ogólnej populacji.
Nie ustalono przydatności testów serologicznych do oceny odpowiedzi immunologicznej na szczepienie. Nie zaleca się wykonywania badań serologicznych w celu oceny odpowiedzi na szczepienie przed podaniem dawki dodatkowej oraz przypominającej.

Jakie najdłuższe odstępy pomiędzy podaniem dwóch dawek szczepionki przeciw COVID-19 można zastosować?
W odniesieniu do całego programu szczepień ochronnych przeciw COVID-19 najdłuższy odstęp czasu dla podania szczepionki Comirnaty (Pfizer BioNTech) i szczepionki Spikevax (Moderna) wynosi 42 dni (jest zgodny z maksymalnym terminem, w którym podawano drugą dawkę szczepionki w badaniach klinicznych. W przypadku szczepionki Vaxzevria (AstraZeneca) najdłuższy odstęp czasu pomiędzy dawkami to 84 dni (zgodnie z zapisem w Charakterystyce Produktu Leczniczego).
Jednak w sytuacjach indywidualnych, kiedy z różnych powodów, np. związanych z przeciwwskazaniami medycznymi lub z powodów organizacyjnych drugiej dawki szczepionki nie podano w ww terminie, należy postępować zgodnie z ogólnymi zasadami dotyczącymi realizacji szczepień ochronnych:
• każda podana dawka szczepionki jest ważna,
• nie rozpoczynamy przerwanego schematu szczepienia od początku,
• uzupełniamy brakującą dawkę szczepionki w pierwszym możliwym terminie, nawet jeżeli odstęp jest dłuższy niż ww.
Zakończenie zalecanego schematu szczepienia, tj. podania 2 dawek szczepionki Comirnaty (Pfizer BioNTech), szczepionki Spikevax (Moderna) oraz szczepionki Vaxzevria (AstraZeneca) jest bardzo ważne, szczególnie w odniesieniu do uzyskania możliwie najlepszej ochrony przed zakażeniem i objawami choroby wywołanej przez wariant Delta wirusa SARS-CoV-2.
Czy należy zachować odstęp czasu pomiędzy szczepieniem przeciw COVID-19 a innym szczepieniem?
Każdą szczepionkę można podać w dowolnym czasie od szczepienia przeciw COVID-19. Nie ma konieczności zachowania jakiegokolwiek odstępu pomiędzy szczepieniami.
Zgodnie z wytycznymi Amerykańskiej Akademii Pediatrii (American Academy of Pediatrics), Centrum Kontroli i Zapobiegania Chorób (Centers for Disease Control and Prevention) oraz lokalnymi wytycznymi kilku krajów w Europie dotyczącymi podawania szczepionek przeciw COVID-19 z innymi szczepionkami, nie ma konieczności zachowania określonego odstępu pomiędzy szczepieniem przeciw COVID-19 oraz innymi szczepieniami. Dotyczy to zarówno szczepień dzieci jak i szczepień dorosłych.
W przypadku szczepień przeciw grypie i szczepień przeciw COVID-19 eksperci wręcz zalecają ich podawanie w czasie tej samej wizyty szczepiennej.
Nie ma konieczności zachowania odstępu czasowego pomiędzy szczepieniem przeciw grypie, a jakimkolwiek innym szczepieniem.
Szczepionki przeciw COVID-19 można podawać w dowolnym czasie przed lub po podaniu innych szczepionek.
Eksperci rekomendują jednoczesne (w czasie jednej wizyty, w dwie różne kończyny) szczepienia przeciw COVID-19 i przeciw grypie wszystkimi dostępnymi na rynku szczepionkami dla danej grupy wiekowej.
W przypadku wątpliwości (np. wystąpienia działań niepożądanych po poprzednich dawkach) należy rozważyć zachowanie bezpiecznego odstępu pomiędzy szczepieniami.
Na początku realizacji programu szczepień przeciw Covid-19 zalecano zachowanie ≥14 dni odstępu pomiędzy podaniem szczepionki przeciw Covid-19 oraz innymi szczepionkami. Wynikało to z ostrożności, a nie z uwagi na jakiekolwiek znane obawy dotyczące wpływu na bezpieczeństwo lub immunogenność szczepionki. Odstęp 14 dni wynikał z procedury badania klinicznego, gdzie takie postępowanie obowiązywało. Szczepionki przeciw COVID-19, tak mRNA jak i wektorowe, nie zawierają zdolnego do replikacji wirusa. Można w ich przypadku zastosować ogólne wymagania dotyczące podawania szczepionek, zgodnie z którymi wymagany odstęp czasu 28 dni, dotyczy jedynie sytuacji, kiedy podajemy dwie żywe szczepionki.
O bezpieczeństwie
Jakie działania niepożądane mogą wystąpić po białkowej szczepionce Nuvaxovid?
W badaniach klinicznych białkowej szczepionki Nuvaxovid najczęściej zgłaszanymi miejscowymi niepożądanymi odczynami poszczepiennymi (NOP) były ból/tkliwość w miejscu wstrzyknięcia, rzadziej zgłaszano zaczerwienienie i obrzęk. Najczęściej zgłaszanymi ogólnoustrojowymi NOP były: zmęczenie i gorsze samopoczucie, ból głowy i mięśni. Większość z nich miała łagodne lub umiarkowane nasilenie i ustępowała do 3 dni po szczepieniu. NOP częściej obserwowano u osób w wieku 12-64 lata niż w wieku ≥65 lat oraz po drugiej dawce szczepionki. U osób w wieku ≥18 lat miejscowe i ogólnoustrojowe NOP obserwowano częściej po podaniu dawki przypominajacej szczepionki Nuvaxovid niż po drugiej dawce schematu podstawowego.
Działania niepożądane które mogą wystąpić po szczepionce mRNA
Po podaniu szczepionki mRNA przeciw COVID-10 mogą wystąpić:
- miejscowe niepożądane odczyny poszczepienne (NOP) (np. ból, obrzęk, zaczerwienienie w miejscu wkłucia, powiększenie okolicznych pachowych węzłów chłonnych po stronie wstrzyknięcia, lub NOP ogólnoustrojowe (np. gorączka, zmęczenie, ból głowy, dreszcze, ból mięśni lub stawów),
- większość ogólnoustrojowych NOP ma charakter łagodny lub umiarkowany, pojawia się w ciągu pierwszych 3 dni po szczepieniu i ustępuje w ciągu 1–2 dni,
- NOP występują częściej i są bardziej nasilone po podaniu drugiej dawki szczepionki oraz u osób młodszych niż u starszych,
- u ozdrowieńców, niektóre NOP (gorączka, dreszcze, ból mięśni) mogą występować częściej po pierwszej dawce szczepionki.
Szczepionka Comirnaty (Pfizer-BioNTech)
Najczęstsze działania niepożądane (zgłoszone w badaniach klinicznych):
- ból w miejscu wstrzyknięcia (>80%),
- zmęczenie (>60%),
- ból głowy (>50%),
- ból mięśni i dreszcze (>30%),
- ból stawów (>20%),
- gorączka i obrzęk w miejscu wstrzyknięcia (>10%).
Działania te miały zazwyczaj nasilenie łagodne lub umiarkowane oraz ustępowały w ciągu 1-2 dni od podania szczepionki.
U osób w podeszłym wieku występowało mniej działań niepożądanych.
Charakterystyce Produktu Leczniczego dla lekarza oraz Ulotce dla pacjenta
Szczepionka Spikevax (Moderna)
Najczęstsze działania niepożądane (zgłoszone w badaniach klinicznych):
- ból w miejscu wstrzyknięcia (92%),
- zmęczenie (70%),
- ból głowy (64,7%),
- ból mięśni (61,5%),
- ból stawów (46,4%),
- dreszcze (45,4%),
- nudności/wymioty (23%),
- obrzęk/tkliwość pod pachą(19,8%),
- gorączka (15,5%),
- obrzęk w miejscu wstrzyknięcia (14,7%)
- zaczerwienienie (10%)
Większość miejscowych i ogólnoustrojowych działań niepożądanych miała nasilenie łagodne lub umiarkowane i ustępowały w ciągu 1-2 dni po szczepieniu. Nieco mnie działań niepożądanych odnotowano u osób w podeszłym wieku.
Niektóre działania niepożądane występowały częściej w młodszych grupach wiekowych. Częstość występowania obrzęku/tkliwości pod pachą, zmęczenia, bólu głowy, bólu mięśni, bólu stawów, dreszczy, nudności/wymiotów i gorączki była większa u osób dorosłych w wieku od 18 do <65 lat niż u osób w wieku 65 lat i starszych.
Miejscowe i ogólne działania niepożądane były zgłaszane częściej po podaniu 2 dawki niż po podaniu 1 dawki.
Charakterystyka Produktu Leczniczego dla lekarza oraz Ulotka dla pacjenta.
- U niektórych osób w okresie po szczepieniu preparatami mRNA (tj. Pfizer/BioNTech, Moderna) odnotowano przypadki zapalenia mięśnia sercowego lub osierdzia. Zdarzenia te najczęściej występowały w ciągu kilku dni po podaniu drugiej dawki szczepionki, głównie u chłopców i młodych mężczyzn, w wieku 12-29 lat. Występowały z ekstremalnie niską częstością. Większość pacjentów wymagała hospitalizacji, w trakcie której ustępowały ostre objawy choroby. Mechanizm rozwoju zapalenia mięśnia sercowego lub osierdzia w okresie po szczepieniu preparatami mRNA nie jest dokładnie poznany.
- Jeżeli po podaniu szczepionki mRNA wystąpi którykolwiek z takich objawów, jak: ból w klatce piersiowej, duszność, uczucie szybkiego bicia serca, trzepotania lub kołatania serca, należy natychmiast zgłosić się do lekarza,
- Wszystkie przypadki zapalenia mięśnia sercowego lub osierdzia, które wystąpią w okresie po szczepieniu COVID-19 należy zgłaszać do systemu rejestracji NOP.
- Eksperci podkreślają, że KORZYŚCI ze szczepienia przeciw COVID-19 preparatami mRNA zdecydowanie przeważają ryzyko związane z występowaniem zapalenia mięśnia sercowego i zapalenia osierdzia po szczepieniu. Dotyczy to populacji objętej szczepieniami, tj. osób ≥12 lat preparatem Pfizer – BioNTech oraz osób ≥18 lat preparatem Moderna.
Co warto wiedzieć o występowaniu zapalenia mięśnia sercowego po szczepieniu przeciw COVID-19 preparatem mRNA?
- Wśród osób, które otrzymały szczepionkę mRNA przeciw COVID-19, w tym Comirnaty (Pfizer-BioNTech) i Spikevax (Moderna), zaobserwowano nieznaczne zwiększenie ryzyka wystąpienia zapalenia mięśnia sercowego lub zapalenia osierdzia w porównaniu z osobami nieszczepionymi.
- Sama choroba COVID-19 wiąże się z istotnie większym ryzykiem zapalenia mięśnia sercowego i innych powikłań kardiologicznych niż szczepienie.
- Grupy ekspertów i oficjalne instytucje jak WHO, CDC, EMA, ECDC podkreślają, że korzyści ze szczepienia chroniącego przed COVID-19 znacznie przewyższają rzadkie ryzyko zapalenia mięśnia sercowego lub osierdzia. Comirnaty i Spikevax są nadal zalecane młodzieży w wieku 12 lat i starszym oraz wszystkim osobom dorosłym.
- Wystąpienie zapalenia osierdzia i mięśnia sercowego po szczepionkach mRNA COVID-19 zgłaszano najczęściej u mężczyzn w wieku poniżej 30 lat i zazwyczaj po drugiej dawce szczepionki.
- Większość przypadków zapalenia mięśnia sercowego i osierdzia związanych ze szczepionką mRNA miała łagodny przebieg i pacjenci szybko wracali do zdrowia. Nadal trwają długoterminowe obserwacje przebiegu choroby.
- Szczepionki wektorowe Vaxzevria (AstraZeneca) ani COVID-19 Vaccine Janssen nie powodują zwiększonego ryzyka wystąpienia zapalenia mięśnia sercowego lub osierdzia. Chociaż zgłaszano przypadki zachorowań po podaniu tej szczepionki, nie były one zgłaszane częściej niż można by się tego spodziewać w przypadku braku szczepień.
- Występujące wcześniej schorzenia kardiologiczne nie są uważane za przeciwwskazanie do szczepienia przeciw COVID-19.
- Osoby, u których w przeszłości występowały którekolwiek z poniższych schorzeń sercowo-naczyniowych, mogą otrzymać szczepionkę mRNA (Comirnaty lub Spikevax), ale powinny skonsultować się z lekarzem rodzinnym, wakcynologiem lub kardiologiem w sprawie najlepszego terminu szczepienia oraz tego, czy zalecane są dodatkowe środki ostrożności:
- niedawno przebyte (tj. w ciągu ostatnich 3 miesięcy) zapalenie mięśnia sercowego lub osierdzia,
- ostra gorączka reumatyczna lub ostra reumatyczna choroba serca (tj. z oznakami aktywnego stanu zapalnego),
- zdekompensowana niewydolność serca.
- Objawy zapalenia mięśnia sercowego lub osierdzia pojawiają się zwykle w ciągu 1-5 dni po podaniu drugiej dawki szczepionki mRNA i mogą obejmować ból w klatce piersiowej, kołatanie serca (nieregularne bicie serca), omdlenia (zasłabnięcia) lub duszności. Osoby, u których wystąpi którykolwiek z tych objawów po podaniu szczepionki mRNA przeciw COVID-19, powinny niezwłocznie zwrócić się po pomoc medyczną.
- W zależności od stopnia ciężkości klinicznej i ryzyka, niektórzy pacjenci mogą wymagać kontroli na oddziale ratunkowym lub pobytu w szpitalu, a niektórym wystarczy porada ambulatoryjna.
- Wstępne badania powinny obejmować EKG i oznaczenie stężenia troponiny we krwi. Pozostałe badania diagnostyczne, w tym badanie radiologiczne klatki piersiowej i inne badania w celu wykluczenia innych przyczyn powinny być wykonane zgodnie ze wskazaniami klinicznymi.
- Zalecenia dotyczące ewentualnych dawek przypominających szczepionki w przyszłości różnią się w zależności od wyników badań:
- kolejne dawki szczepionki mRNA przeciwko COVID-9 można podać osobom, u których podejrzewano zapalenie osierdzia, ale u których stwierdzono prawidłowe wyniki EKG, troponiny i markerów stanu zapalnego oraz u których przez co najmniej 6 tygodni nie wystąpiły żadne objawy. Dotyczy to również osób z klinicznym rozpoznaniem zapalenia osierdzia pomimo prawidłowych wyników badań.
- u osób, u których potwierdzono zapalenie mięśnia sercowego przypisywane szczepionce Comirnaty lub Spikevax, powinno się odroczyć podanie kolejnych dawek szczepionki mRNA przeciwko COVID-19, a jeśli są w wieku > 18 lat, można w indywidualnych przypadkach rozważyć szczepionkę Vaxzevria, po wyzdrowieniu z objawów.
Szczepionka mRNA przeciw COVID-19, jak każda szczepionka może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Gdzie można zgłosić NOP po szczepieniu przeciw COVID-19?
NOP po szczepieniu przeciw COVID-19 można zgłosić do:
- lekarza, który po rozpoznaniu NOP zgłasza go do inspekcji sanitarnej (elektronicznie za pośrednictwem aplikacji gabinet.gov.pl). Od 6 stycznia 2021 roku obowiązuje rozporządzenie Ministra Zdrowia z dnia 31 grudnia 2020 roku zmieniające rozporządzenie w sprawie niepożądanych odczynów poszczepiennych oraz kryteriów ich rozpoznawania (Dz.U. z 2020 r. poz.13), gdzie wskazano zmienioną drogę przesyłania zgłoszenia podejrzenia lub rozpoznania NOP i sposób gromadzenia tych zgłoszeń przez właściwe organy inspekcji sanitarnej. Rozporządzenie to wprowadza również nowy wzór karty zgłoszenia NOP, która uwzględnia szczepienie przeciwko COVID-19.
- każdy może zgłosić działanie niepożądane do Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, Al. Jerozolimskie 181C, 02-222 Warszawa, tel.: +48 22 49 21 301, faks: +48 22 49 21 309, strona internetowa: https://smz.ezdrowie.gov.pl
- każdy może zgłosić działanie niepożądane bezpośrednio do podmiotu odpowiedzialnego (dane kontaktowe podane są na ulotce dla pacjenta danej szczepionki).
Gdzie można znaleźć informacje na temat liczby NOP zgłoszonych po szczepieniach przeciw COVID-19?
Informacje o liczbie i rodzaju niepożądanych odczynów poszczepiennych (NOP) po szczepieniach przeciw COVID-19, zgłoszonych przez lekarzy do Państwowej Inspekcji Sanitarnej można znaleźć w 2 miejscach:
- na stronie Szczepimysie poświęconej programowi szczepień przeciw COVID-19, gdzie dostępne są bieżące raporty dotyczące niepożądanych odczynów poszczepiennych zgłoszonych po szczepieniach przeciw COVID-19.
- Na stronie NIZP PZH-PIB dostępne są okresowe wyniki analizy NOP.
Analiza obejmująca okres 27.12.2020-27.12.2021.
Aktualna analiza obejmuje okres od 27.12.2020 do 15.01.2022 (80% zarejestrowanych zgłoszeń). Wykonano 49 264 863 szczepień przeciw COVID-19. Zgłoszono 17 528 niepożądanych odczynów poszczepiennych (NOP) i niepożądanych zdarzeń medycznych (NZM). Częstość zgłoszonych NOP i NZM ogółem wynosi 0,05%.

-
 Jak działa szczepionka mRNA?
Plik otwiera się w nowej karcie
Jak działa szczepionka mRNA?
Plik otwiera się w nowej karcie
-
 Jak działa szczepionka wektorowa?
Plik otwiera się w nowej karcie
Jak działa szczepionka wektorowa?
Plik otwiera się w nowej karcie
-
 Kiedy pojawia się odporność po szczepieniu?
Plik otwiera się w nowej karcie
Kiedy pojawia się odporność po szczepieniu?
Plik otwiera się w nowej karcie
-
 NOP po szczepionkach przeciw COVID-19
Plik otwiera się w nowej karcie
NOP po szczepionkach przeciw COVID-19
Plik otwiera się w nowej karcie
-
 Skład szczepionki mRNA przeciw COVID-19
Plik otwiera się w nowej karcie
Skład szczepionki mRNA przeciw COVID-19
Plik otwiera się w nowej karcie
-
 Skład szczepionki mRNA przeciw COVID-19
Plik otwiera się w nowej karcie
Skład szczepionki mRNA przeciw COVID-19
Plik otwiera się w nowej karcie
-
 Skład szczepionki wektorowej przeciw COVID-19
Plik otwiera się w nowej karcie
Skład szczepionki wektorowej przeciw COVID-19
Plik otwiera się w nowej karcie
-
 Szczepienia przeciw COVID-19 nastolatków
Plik otwiera się w nowej karcie
Szczepienia przeciw COVID-19 nastolatków
Plik otwiera się w nowej karcie
-
 Szczepionki ratują życie
Plik otwiera się w nowej karcie
Szczepionki ratują życie
Plik otwiera się w nowej karcie
-
 Bezpieczna szczepionka 1
Plik otwiera się w nowej karcie
Bezpieczna szczepionka 1
Plik otwiera się w nowej karcie
-
 Bezpieczna szczepionka 2
Plik otwiera się w nowej karcie
Bezpieczna szczepionka 2
Plik otwiera się w nowej karcie
-
 Podział szczepionek przeciw COVID-19
Plik otwiera się w nowej karcie
Podział szczepionek przeciw COVID-19
Plik otwiera się w nowej karcie
-
 Szczepionki przeciw COVID-19 są bezpieczne
Plik otwiera się w nowej karcie
Szczepionki przeciw COVID-19 są bezpieczne
Plik otwiera się w nowej karcie
-
 Bezpieczeństwo szczepionek przeciw COVID-19
Plik otwiera się w nowej karcie
Bezpieczeństwo szczepionek przeciw COVID-19
Plik otwiera się w nowej karcie
-
 Szczepienia dzieci i młodzieży
Plik otwiera się w nowej karcie
Szczepienia dzieci i młodzieży
Plik otwiera się w nowej karcie
-
 Covid-19 (ściąga) (pdf)
Plik otwiera się w nowej karcie
Covid-19 (ściąga) (pdf)
Plik otwiera się w nowej karcie
-
 Covid-19 (ściąga) (jpg)
Plik otwiera się w nowej karcie
Covid-19 (ściąga) (jpg)
Plik otwiera się w nowej karcie
-
 Szczepienia przeciw COVID-19 w sezonie 2024/2025
Plik otwiera się w nowej karcie
Szczepienia przeciw COVID-19 w sezonie 2024/2025
Plik otwiera się w nowej karcie
-
 Bezpieczeństwo szczepień COVID-19 w okresie ciąży
Plik otwiera się w nowej karcie
Bezpieczeństwo szczepień COVID-19 w okresie ciąży
Plik otwiera się w nowej karcie
- Transmission of SARS-CoV-2: implications for infection prevention precautions. (podsumowanie danych naukowych z 9 lipca 2020).
- Harrison AG, Lin T, Wang P. Mechanisms of SARS-CoV-2 Transmission and Pathogenesis. Trends Immunol. 2020 Dec;41(12):1100-1115.
- Rastawicki W, Juszczyk G, Gierczyński R, Zasada A.A. Comparison of anti-SARS-CoV-2 IgG and IgA antibody responses post complete vaccination, 7 months later and after 3rd dose of the BNT162b2 vaccine in healthy adults. Journal of Clinical Virology 2022; 152 105193.
- Rastawicki W, Płaza K. The level of protective post-vaccination antibodies in NIPH-NIH employees after administration of Pfizer vaccine against COVID-19. Przegląd Epidemiologiczny 2021, doi 10.32394/pe.75.01.
- Wełnicki M, Mamcarz A, Kuchar E, Mitkowski P, Jaroszewicz J, Tomasiewicz K, Gąsior M, Leszek P, Kamiński KA, Wysocki J. The Impact of COVID-19 and the Practical Importance of Vaccinations and Nirmatrelvir/Ritonavir for Patients with Cardiovascular Disease. Vaccines (Basel). 2025 May 23;13(6):554.
Przeczytaj również

Refundacja szczepionki przeciw ludzkiemu wirusowi brodawczaka (HPV)
CZYTAJ WIĘCEJ
Eksperci potwierdzają bezpieczeństwo i wysoką skuteczność szczepień przeciwko HPV realizowanych w szkołach
CZYTAJ WIĘCEJ
Kto i gdzie może w Polsce zgłaszać NOP?
CZYTAJ WIĘCEJ



