Szczepionka przeciw COVID-19
Jaka jest różnica pomiędzy szczepionką mRNA a dotychczas stosowanymi szczepionkami?
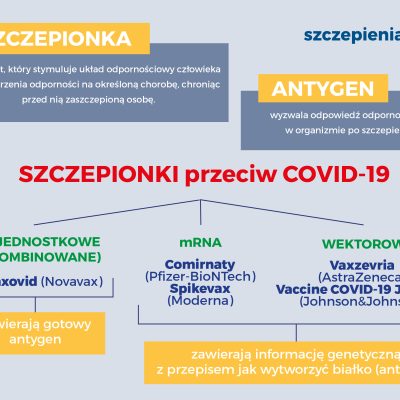
Różnica między szczepionką mRNA a dotychczas stosowanymi szczepionkami dotyczy sposobu i miejsca gdzie produkowane jest białko pełniące rolę antygenu w szczepionce. W dotychczas stosowanych szczepionkach podawaliśmy gotowe białka (antygeny) lub ich fragmenty, które stymulowały organizm do wytworzenia przeciwciał neutralizujących oraz odpowiedzi na poziomie komórkowym. W przypadku szczepionek mRNA do organizmu podajemy tylko informację genetyczną o tym jak dane białko powinno być wytworzone. Sama produkcja białka zachodzi już w naszych komórkach.
Innymi słowy w szczepionkach mRNA nie podajemy gotowego antygenu, a dokładny przepis na jego przygotowanie w postaci mRNA kodującego informację o białku pełniącym funkcję antygenu.
Jak działają szczepionki białkowe przeciw COVID-19?
Co to są szczepionki białkowe?
W szczepionkach białkowych wykorzystuje się te fragmenty wirusa, które zostaną rozpoznane przez układ odpornościowy i wywołują reakcję immunologiczną. Szczepionki te nie zawierają całego wirusa ani innego wirusa.
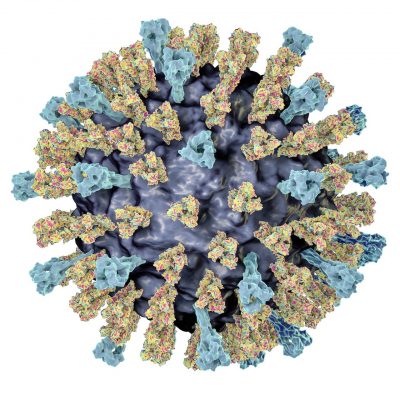
Na powierzchni koronawirusa SARS-CoV-2 znajdują się małe wypustki nazywane białkami kolca. Dzięki nim wirus wnika do komórki i wywołuje chorobę.
Szczepionki białkowe zawierają fragmenty białkowe wytworzone w laboratorium. Dzięki tym fragmentom układ odpornościowy rozpoznaje wirusa i go zwalcza. W efekcie albo choroba nie rozwija się, albo daje jedynie łagodne objawy.
Wykorzystywanie w szczepionkach fragmentów wirusa, np. białek to szeroko stosowana i ugruntowana technologia.
Co dzieje się w organizmie po podaniu szczepionki białkowej?
Szczepionka białkowa przeciw COVID-19 podawana jest drogą domięśniową. Po podaniu preparatu organizm styka się z białkiem wirusa. Układ odpornościowy wykrywa obce białko i wytwarza atakujące go przeciwciała i komórki odpornościowe. Dzięki temu organizm eliminuje obce białko.
Jeżeli dojdzie do zakażenia koronawirusem, układ odpornościowy będzie pamiętał, jak go zniszczyć.
Choroba COVID-19 nie rozwinie się lub wywoła jedynie łagodne objawy.
Szczepionki białkowe są stosowane od wielu lat i są bezpieczne. Ich produkcja jest stosunkowo łatwa. Można je przechowywać przez wiele miesięcy w lodówce (2-8▫C).
Szczepionka mRNA nie zawiera wirusa ani jego fragmentów. Zawiera tylko informację genetyczną (mRNA), dzięki której białko (antygen) wirusa będzie wytworzone w naszych komórkach, po podaniu szczepionki.
-
 Jak działa szczepionka mRNA?
Plik otwiera się w nowej karcie
Jak działa szczepionka mRNA?
Plik otwiera się w nowej karcie
-
 Jak działa szczepionka wektorowa?
Plik otwiera się w nowej karcie
Jak działa szczepionka wektorowa?
Plik otwiera się w nowej karcie
-
 Kiedy pojawia się odporność po szczepieniu?
Plik otwiera się w nowej karcie
Kiedy pojawia się odporność po szczepieniu?
Plik otwiera się w nowej karcie
-
 NOP po szczepionkach przeciw COVID-19
Plik otwiera się w nowej karcie
NOP po szczepionkach przeciw COVID-19
Plik otwiera się w nowej karcie
-
 Skład szczepionki mRNA przeciw COVID-19
Plik otwiera się w nowej karcie
Skład szczepionki mRNA przeciw COVID-19
Plik otwiera się w nowej karcie
-
 Skład szczepionki mRNA przeciw COVID-19
Plik otwiera się w nowej karcie
Skład szczepionki mRNA przeciw COVID-19
Plik otwiera się w nowej karcie
-
 Skład szczepionki wektorowej przeciw COVID-19
Plik otwiera się w nowej karcie
Skład szczepionki wektorowej przeciw COVID-19
Plik otwiera się w nowej karcie
-
 Szczepienia przeciw COVID-19 nastolatków
Plik otwiera się w nowej karcie
Szczepienia przeciw COVID-19 nastolatków
Plik otwiera się w nowej karcie
-
 Szczepionki ratują życie
Plik otwiera się w nowej karcie
Szczepionki ratują życie
Plik otwiera się w nowej karcie
-
 Bezpieczna szczepionka 1
Plik otwiera się w nowej karcie
Bezpieczna szczepionka 1
Plik otwiera się w nowej karcie
-
 Bezpieczna szczepionka 2
Plik otwiera się w nowej karcie
Bezpieczna szczepionka 2
Plik otwiera się w nowej karcie
-
 Podział szczepionek przeciw COVID-19
Plik otwiera się w nowej karcie
Podział szczepionek przeciw COVID-19
Plik otwiera się w nowej karcie
-
 Szczepionki przeciw COVID-19 są bezpieczne
Plik otwiera się w nowej karcie
Szczepionki przeciw COVID-19 są bezpieczne
Plik otwiera się w nowej karcie
-
 Bezpieczeństwo szczepionek przeciw COVID-19
Plik otwiera się w nowej karcie
Bezpieczeństwo szczepionek przeciw COVID-19
Plik otwiera się w nowej karcie
-
 Szczepienia dzieci i młodzieży
Plik otwiera się w nowej karcie
Szczepienia dzieci i młodzieży
Plik otwiera się w nowej karcie
-
 Covid-19 (ściąga) (pdf)
Plik otwiera się w nowej karcie
Covid-19 (ściąga) (pdf)
Plik otwiera się w nowej karcie
-
 Covid-19 (ściąga) (jpg)
Plik otwiera się w nowej karcie
Covid-19 (ściąga) (jpg)
Plik otwiera się w nowej karcie
-
 Szczepienia przeciw COVID-19 w sezonie 2024/2025
Plik otwiera się w nowej karcie
Szczepienia przeciw COVID-19 w sezonie 2024/2025
Plik otwiera się w nowej karcie
-
 Bezpieczeństwo szczepień COVID-19 w okresie ciąży
Plik otwiera się w nowej karcie
Bezpieczeństwo szczepień COVID-19 w okresie ciąży
Plik otwiera się w nowej karcie
- Transmission of SARS-CoV-2: implications for infection prevention precautions. (podsumowanie danych naukowych z 9 lipca 2020).
- Harrison AG, Lin T, Wang P. Mechanisms of SARS-CoV-2 Transmission and Pathogenesis. Trends Immunol. 2020 Dec;41(12):1100-1115.
- Rastawicki W, Juszczyk G, Gierczyński R, Zasada A.A. Comparison of anti-SARS-CoV-2 IgG and IgA antibody responses post complete vaccination, 7 months later and after 3rd dose of the BNT162b2 vaccine in healthy adults. Journal of Clinical Virology 2022; 152 105193.
- Rastawicki W, Płaza K. The level of protective post-vaccination antibodies in NIPH-NIH employees after administration of Pfizer vaccine against COVID-19. Przegląd Epidemiologiczny 2021, doi 10.32394/pe.75.01.
- Wełnicki M, Mamcarz A, Kuchar E, Mitkowski P, Jaroszewicz J, Tomasiewicz K, Gąsior M, Leszek P, Kamiński KA, Wysocki J. The Impact of COVID-19 and the Practical Importance of Vaccinations and Nirmatrelvir/Ritonavir for Patients with Cardiovascular Disease. Vaccines (Basel). 2025 May 23;13(6):554.