
Szczepionka przeciw rotawirusom
O chorobie
Co to jest infekcja rotawirusowa?
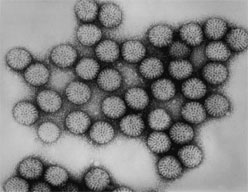
Rotawirusy (wirusy należące do rodziny łac. Reoviridae) są najczęstszym czynnikiem wywołującym biegunki zakaźne u niemowląt i małych dzieci do 5 roku życia. Zachorowania dotyczą najczęściej dzieci od 4 do 24 miesiąca życia. Najciężej biegunki rotawirusowe przebiegają u dzieci poniżej 6 miesiąca życia, ponieważ ich organizm ulega szybko odwodnieniu.
U dorosłych przebieg infekcji rotawirusowej jest zwykle bezobjawowy.
Okres wylęgania infekcji rotawirusowej wynosi 12-96 godzin.
Zakażenie rotawirusami następuje drogą fekalno-oralną lub pośrednio przez przedmioty. Po przedostaniu się do organizmu, wirusy uszkadzają nabłonek kosmków jelitowych, wywołując stan zapalny żołądka i jelit.
Jakie są objawy infekcji rotawirusowej?
U osób zakażonych rotawirusami w krótkim czasie dochodzi do stanu zapalnego przewodu pokarmowego. Do głównych objawów infekcji rotawirusowej należą:
- gorączka – do 40oC,
- wymioty – często obfite,
- biegunka – częsta, wodnista, żółtozielone stolce, zwykle bez krwi i śluzu,
- brak łaknienia,
- odwodnienie.
Jak poważne mogą być objawy infekcji rotawirusowej?
Przebieg infekcji rotawirusowej zależy od serotypu wirusa, wieku dziecka, stanu układu odpornościowego oraz sposobu odżywiania. Utrata płynów i elektrolitów związana z wymiotami i biegunką może doprowadzić do ciężkiego odwodnienia, wstrząsu hipowolemicznego, a przy braku odpowiedniego leczenia nawet do zgonu.
Jedynym sposobem terapii jest leczenie objawowe, tj. nawadnianie doustne i dożylne.
Jak wiele zachorowań na infekcje rotawirusowe występuje w Polsce?
Zgodnie z danymi NIZP-PZH liczba zachorowań na wirusowe zakażenia jelitowe wywołane przez rotawirusy jest różna w poszczególnych latach (w ciągu ostatnich 5- lat odnotowano najmniej 21 258 zachorowań w 2016 roku do 33 944 zachorowań w 2015 roku). W 2017 roku zarejestrowano 32 995 zachorowań, a w 2018 roku – 23 263 zachorowania. W 2018 roku zapadalność w całej populacji wynosiła 60,6/100 tys., a w 2017 roku – 85,8/100 tys. Najwięcej zachorowań, występowało u dzieci do 4 roku życia, w 2018 roku zapadalność w tej grupie wynosiła 967,8/100 tys., a w 2017 roku- 1377,6/100 tys. W ponad 90% zgłoszenia dotyczą przypadków hospitalizowanych.
Według danych NFZ w 2017 roku hospitalizowano 25 214 dzieci, a w 2018 roku 17 859 dzieci z powodu nieżytu jelitowego wywołanego przez rotawirusy. Natomiast z powodu nieżytu żołądkowo-jelitowego o prawdopodobnym lub potwierdzonym podłożu infekcyjnym w 2017 roku hospitalizowano 53 707 dzieci, a w 2018 roku 46 462 dzieci, w tym głównie dzieci do 6 roku życia.
Rotawirusy w Polsce w latach 2009 -2024 – epidemiologia (pdf)
Częstość infekcji rotawirusowych, oszacowana przez polskich epidemiologów, uwzględniająca dane Narodowego Funduszu Zdrowia oraz Głównego Inspektoratu Sanitarnego (dane dotyczące zakażeń szpitalnych) szacowana jest na około 200.000 zachorowań rocznie.
Gdzie i jak często infekcje rotawirusowe występują na świecie?
Liczba infekcji rotawirusowych oceniana jest na 111 mln na świecie oraz 3 mln w Europie. Światowa Organizacja Zdrowia ocenia, że każdego roku na świecie z powodu zakażeń rotawirusowych umiera 520 000 dzieci w wieku do 5 lat. W Europie każdego roku około 75 000-150 000 dzieci w wieku poniżej pięciu lat jest hospitalizowanych z powodu biegunki rotawirusowej. Ponadto, nawet 4 razy więcej dzieci wymaga pomocy w placówkach ambulatoryjnych.
W klimacie umiarkowanym szczyt zachorowań przypada na miesiące zimowe. W krajach, gdzie różnice temperatur są mniejsze, sezonowość zachorowań jest mniej wyraźna.
-
 Rotawirusy w Polsce w latach 2009 -2024
Plik otwiera się w nowej karcie
Rotawirusy w Polsce w latach 2009 -2024
Plik otwiera się w nowej karcie
-
 Szczepienie przeciw rotawirusom - wiek dziecka
Plik otwiera się w nowej karcie
Szczepienie przeciw rotawirusom - wiek dziecka
Plik otwiera się w nowej karcie
-
 Szczepienia przeciw rotawirusom. Okno czasowe
Plik otwiera się w nowej karcie
Szczepienia przeciw rotawirusom. Okno czasowe
Plik otwiera się w nowej karcie
-
 Szczepienia przeciw rotawirusom. Podanie pierwszej dawki
Plik otwiera się w nowej karcie
Szczepienia przeciw rotawirusom. Podanie pierwszej dawki
Plik otwiera się w nowej karcie
-
 Główne powody dla których warto dziecko zaszczepić przeciw rotawirusom
Plik otwiera się w nowej karcie
Główne powody dla których warto dziecko zaszczepić przeciw rotawirusom
Plik otwiera się w nowej karcie
-
 Dodatkowe korzyści ze szczepienia przeciw rotawirusom (1)
Plik otwiera się w nowej karcie
Dodatkowe korzyści ze szczepienia przeciw rotawirusom (1)
Plik otwiera się w nowej karcie
-
 Dodatkowe korzyści ze szczepienia przeciw rotawirusom (2)
Plik otwiera się w nowej karcie
Dodatkowe korzyści ze szczepienia przeciw rotawirusom (2)
Plik otwiera się w nowej karcie
-
 Rotawirusy (ściąga)
Plik otwiera się w nowej karcie
Rotawirusy (ściąga)
Plik otwiera się w nowej karcie
-
 Rotawirusy (ściąga)
Plik otwiera się w nowej karcie
Rotawirusy (ściąga)
Plik otwiera się w nowej karcie
-
 Rotawirusy. 6 powodów dla których warto zaszczepić dziecko
Plik otwiera się w nowej karcie
Rotawirusy. 6 powodów dla których warto zaszczepić dziecko
Plik otwiera się w nowej karcie
-
 Szczepienie przeciw rotawirusom
Plik otwiera się w nowej karcie
Szczepienie przeciw rotawirusom
Plik otwiera się w nowej karcie
-
 Główne powody dla których warto zaszczepić dziecko przeciw rotawirusom
Plik otwiera się w nowej karcie
Główne powody dla których warto zaszczepić dziecko przeciw rotawirusom
Plik otwiera się w nowej karcie
- Abbasi J. After Rotavirus Vaccine, Australia’s Type 1 Diabetes Incidence Declines. JAMA 2019;321(13):1241-1242.
- Aldean J.A. i wsp. Recommendations for vaccination against ROTAvirus in PREMature newborns (ROTAPREM). An Pediatr (Barc) 2019;91:207.
- Anderson E.J., Weber S.G., „Rotavirus infection in adults”, Lancet Infect Dis 2004,4(2): 91-9.
- Bernstein D.I. i wsp. Rotavirus overview. Pediatr Infect Dis 2009;28:50-53.
- Prevention of rotavirus gastroenteritis among infants and children: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR 2009;58(No.RR-2).
- Diez-Domingo i wsp. Primary care-based surveillance to estimate the burden of rotavirus gastroenteritis among children aged less than 5 years in six European countries (SPRIK). Eur J Pediatr 2011;170:213-222.
- Esposito S. i wsp. Rotarix and RotaTeq administration to preterm infants in the neonatal intensive care unit: Review of available evidence. Vaccine 2018;36:5430-5445.
- European Centre for Disease Prevention and Control. Expert opinion on rotavirus vaccination in infancy, ECDC, 2017.
- Fischer T.K., Bresee J.S., Glass R.I., „Rotavirus vaccines and the prevention of hospital-acquired diarrhea in children”, Vaccine 2004; 22 Suppl 1: S 49-54.
- Hungerford D. i Iturriza-Gómara M. EuroRotaNet; Annual report 2018, September 2019.
- Korycka M., „Szczepionka przeciwko zakażeniu rotawirusami”, „Wakcynologia”, wyd. II, red. W. Magdzik i wsp., J Medica Press, 2007, str. 499-502.
- Kuchar E. i wsp. Rotawirusy jako czynnik etiologiczny zakażeń szpitalnych w Polsce- przegląd systematyczny z metaanalizą 11 badań. Przegl Epidemiol 2012;66:409-415.
- Mrukowicz J. i wsp. Szczepienie wcześniaków przeciwko rotawirusom w szpitalu. Wytyczne Polskiego Towarzystwa Wakcynologii. Medycyna Praktyczna-Szczepienia 2019;2;1-8.
- Pickering L.K., Baker C.J., Long S.S., McMillan J.A., eds. Red Book: 2006 Report of the Committee on Infectious Diseases. 27th ed. Elk Grove Village, IL: American Academy of Pediatrics, 2006.
- Poelaert i wsp. A review of recommendations for rotavirus vaccination in Europe: Arguments for change. Vaccine 2018;36:2243-53.
- Pollard S.L. i wsp. Estimating the herd immunity effect of rotavirus vaccine. Vaccine 2015;33:3795-3800.
- Rekomendacja Prezesa Agencji Oceny Technologii Medycznych i Taryfikacji w sprawie zasadności stosowania w powszechnych szczepieniach szczepionki przeciwko rotawirusom (z dnia 4 października 2019 r.).
- Rosillon D. i wsp. Risk of intussusception after rotavirus vaccination: meta-analysis of postlicensure studies. Pediatr Infect Dis J 2015;34:763-768.
- Sabbe M. i wsp. Sustained low rotavirus activity and hospitalisation rates in the post-vaccination era in Belgium, 2007 to 2014. Euro Surveill 2016;21(27): pii=30273.
- Soriano-Gabarro M., Mrukowicz J., Vesikari T., Verstraeten T., „Burden of rotavirus disease in European Union countries”, Pediatr Infect Dis J 2006; 25 (1 Suppl): S7-S11.
- Stanowisko WHO dot. szczepionek przeciwko rotawirusom w języku angielskim i francuskim, Weekly Epidemiological Record No. 32, 2007, 82, str. 285–296.
- Tran A.N. i wsp. Impact on affected families and society of severe rotavirus infections in Swedish children assessed in a prospective cohort study. Infect Dis (Lond) 2018;50:361-371.
- Vesikari T. i wsp. ESPID consensus recommendation for rotavirus recommendation for rotavirus vaccination in Europe. J Pediatr Infect Dis 2015; 34:635-643.
- WHO. Post-marketing surveillance of rotavirus vaccine safety. WHO/IVB/09-01.
- Vaccine in National Immunization Programme Update. January 2020 .
- Załęski A. i wsp. Biegunka rotawirusowa – możliwe korzyści z wprowadzenia powszechnych szczepień przeciwko rotawirusom do PSO w Polsce. Standardy Medyczne Pediatria 2018; 2.








