
Na całym świecie wznowiono badania kliniczne wektorowej szczepionki przeciw COVID-19
Badania kliniczne wektorowej szczepionki przeciw COVID-19 opracowywanej przez Uniwersytet Oksfordzki oraz firmę AstraZeneka zostały wznowione, wszędzie gdzie były prowadzone na świecie, a organy regulacyjne w Stanach Zjednoczonych, Wielkiej Brytanii, Brazylii, RPA i Japonii potwierdziły, że wznowienie badań jest bezpieczne. Jako ostatnia 23.10.2020 wypowiedziała się Amerykańska Agencja ds. Rejestracji Żywności i Leków (Food and Drug Administration, FDA) potwierdzając, że zaawansowane badania kliniczne 3 fazy szczepionki wektorowej firmy AstraZeneka mogą być bezpiecznie kontynuowane.
Wcześniej, z powodu wystąpienia poważnego działania niepożądanego u jednego z uczestników badania prowadzonego w Wielkiej Brytanii, firma AstraZeneca zdecydowała o wstrzymaniu 3 fazy badań klinicznych szczepionki wektorowej prowadzonych w różnych miejscach na świecie. Decyzja dotyczącą wstrzymania nastąpiła w wyniku standardowego procesu przeglądu zdarzeń dotyczących bezpieczeństwa badań klinicznych.
Profesor Andrew Pollard z zespołu badawczego Uniwersytetu Oksfordzkiego powiedział: „Jesteśmy bardzo zadowoleni, że FDA doszła do tego samego wniosku, co inne agencje nadzorujące badania kliniczne na świecie, potwierdzając, że badanie kliniczne można bezpiecznie kontynuować nie tylko w Wielkiej Brytanii, Brazylii, RPA, Japonii, ale również w Stanach Zjednoczonych. Dzięki temu możliwe są badania kliniczne łącznie na grupie 50 000 ochotników. Będziemy nadal przestrzegać naszych rygorystycznych procedur bezpieczeństwa, działając tak szybko, jak to możliwe, aby opracować szczepionkę, która pomoże opanować strasznego wirusa SARS-CoV-2”.
W związku z tym, że badania 3 fazy dotyczą dużych grup badanych, występowanie u niektórych uczestników badania zaburzeń zdrowia, jest prawdopodobne. Każdy przypadek musi być dokładnie oceniony, czy dany objaw związany jest z podaniem szczepionki, czy stanowi tylko koincydencję czasową.
Badacze nadzorujący badania kliniczne 3 fazy oceniają, że wyniki będą udostępniane agencjom rejestrującym w grudniu 2020 roku. W przypadku pozytywnego scenariusza, decyzji agencji rejestrującej o dopuszczeniu do obrotu (np. Europejskiej Agencji Leków) szczepionka wejdzie na rynek na początku 2021 roku.
Przeczytaj również
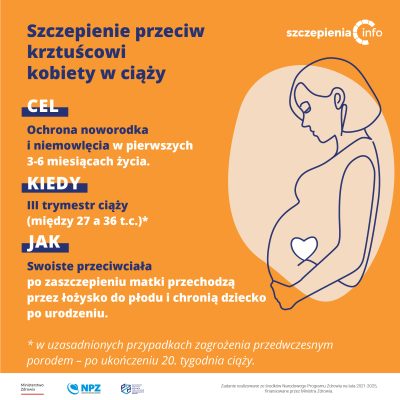
Dlaczego kobiecie w ciąży zaleca się szczepienie przeciw krztuścowi?
CZYTAJ WIĘCEJ
Jak prowadzone są szczepienia przeciw grypie w sezonie 2025/2026?
CZYTAJ WIĘCEJ
Region Europejski WHO od 20 lat wolny od poliomyelitis
CZYTAJ WIĘCEJ

